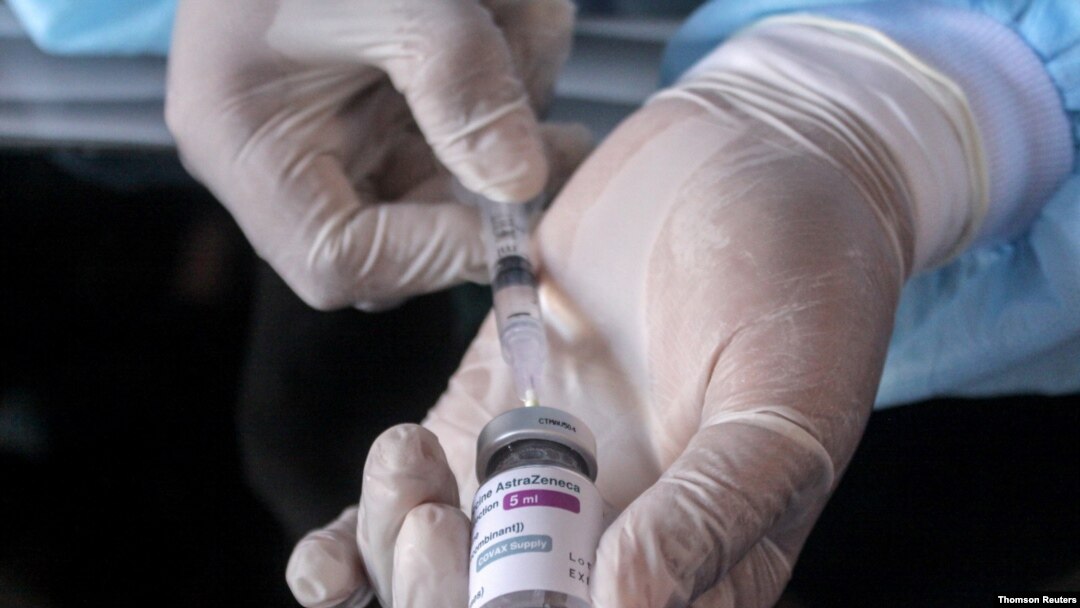
AstraZeneca могла використати деякі «застарілі дані» в випробуваннях свого прототипу вакцини. Таке побоювання виникло у Правління з нагляду за безпекою даних США, незалежної експертної групи, яка розглядає дані досліджень прототипів вакцин, заявив Національний інститут США з алергій та вірусних хвороб.
Заяву було видано у вівторок, на наступний день після того, як компанія AstraZeneca оприлюднила результати клінічних досліджень свого прототипу вакцини у США.
Дивіться також: AstraZeneca: Випробування у США підтвердили дієвість вакцини і не виявили вищого ризику тромбів
Правління з нагляду за безпекою даних США «висловило занепокоєння тим, що AstraZeneca, можливо, включила застарілу інформацію випробувань, що могло надати неповну картину даних із ефективності», заявив Національний інститут США з алергій та вірусних хвороб.
В установі закликали компанію співпрацювати із правлінням «задля перегляду даних з ефективності і забезпечити, щоб найбільш точні сучасні дані були доступні громадськості».
В понеділок AstraZeneca оприлюднила результати випробування свого прототипу вакцини у Сполучених Штатах, а також у Чилі та Перу за участі 32 4499 добровольців. Результати виявили, що прототип вакцини на 79% запобігав симптоматичним захворюванням на COVID-19 і на 100% дозволяла уникати важкого перебігу хвороби й потреб госпіталізації.
Дані цих випробувань будуть подані Федеральній адміністрації з контролю над продуктами харчування та ліками США для отримання дозволу на використання вакцини у Сполучених Штатах, заявили в компанії.
Дивіться також: Темпи вакцинування в Україні – серед найповільніших у світі. Відео
Your browser doesn’t support HTML5
Темпи вакцинування в Україні – серед найповільніших у світі. Відео